“佐米”类药,多家企业在研
原标题:“Zomi”药物,多家公司在研
 < /p>
< /p>
□Wang Yuheng
近日,注射用卡非佐米已获条件批准上市,联合地塞米松用于治疗复发或难治性(R/R)多发性骨髓瘤成人患者( MM) 过去至少接受过两种治疗,包括蛋白酶体抑制剂和免疫调节剂。
卡非佐米是一种蛋白酶体抑制剂。蛋白酶体可以分解受损或不再需要的蛋白质,从而在细胞功能和生长中发挥重要作用。研究表明,卡非佐米可抑制蛋白酶体,导致细胞内蛋白质过度积累。通过这种抑制作用,卡非佐米可以导致一些细胞死亡,特别是对于通常含有大量异常蛋白质的骨髓瘤细胞。该药物最初由 Proteolix 开发。 2009年,Onyx收购Proteolix获得该产品。 2012 年 7 月 20 日获得美国 FDA 批准,用于接受至少两种药物(硼替佐米和免疫调节剂)。 ) 先前接受过治疗的多发性骨髓瘤患者;后来,他们被批准联合来那度胺和地塞米松治疗先前接受过 1 至 3 次治疗的复发性 MM 患者。 2013年8月27日,安进以104亿美元收购Onix Pharmaceuticals,获得Carfilzomib的专利权。百济神州通过与安进的战略合作,获得 Carfilzomi 在中国的授权。
多发性骨髓瘤是一种恶性血液肿瘤,起源于骨髓中浆细胞的异常增殖,从而中断其正常的细胞功能和程序。 MM是第二常见的血液系统恶性肿瘤,约占所有恶性肿瘤的1%和血液系统恶性肿瘤的13%。许多 MM 患者在确诊时已经发展到晚期,近 20% 的患者在初始治疗后可能出现疾病复发。据估计,2016年全球大约有新发MM病例和MM死亡病例。 MM 的发病率在男性和老年人(55 至 74 岁之间)中较高。在疾病控制不佳的情况下,MM还会引起病理性骨折、贫血等并发症。
第一个上市的蛋白酶体抑制剂是Brotezomib,它于1998年12月首次报道,2003年被美国FDA批准用于治疗多发性骨髓瘤,在世界范围内广受欢迎。作为第一代20S蛋白酶体抑制剂,硼替佐米已广泛应用于多发性骨髓瘤的治疗,是该适应症的一线药物;然而,它目前具有很强的耐药性。
与全球销售趋势相反,多年来国内硼替佐米的销售量持续增长。 2019年,硼替佐米在全国主要样本医院的销售额达到5.07亿元。 Carfilzomib 是继硼替佐米之后 FDA 批准的第二种蛋白酶体抑制剂。据统计,卡非佐米全球销售额逐年增长,2020年销售额达到10.65亿美元。
硼替佐米和卡非佐米获批上市后,千禧制药提交了类似新药的上市申请。药物伊沙佐米在美国和欧洲,并于2015年被美国FDA批准上市。伊沙佐米最大的优势在于,它是同类产品中第一个口服治疗药物,真正解决了临床需求,为后续联合开发口服药物奠定了重要基础。 2019年,Ishazomi全球年销售额达到7.12亿美元。
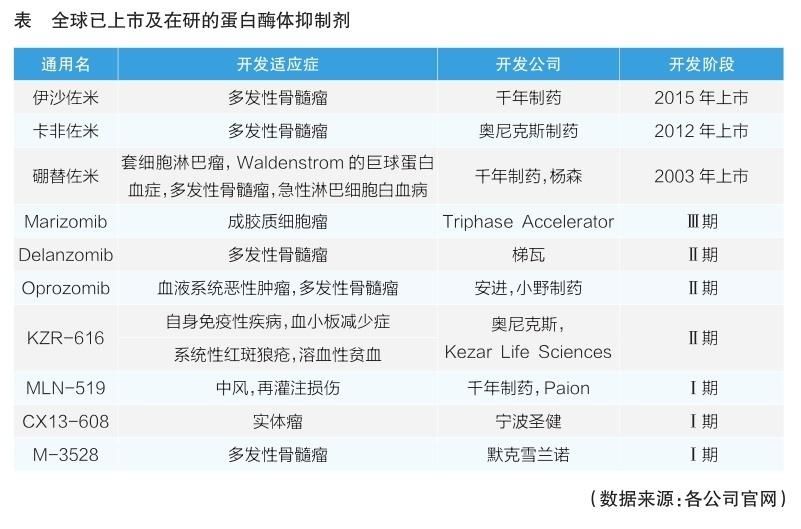
除了列出的三个“Zomi”蛋白酶体抑制剂外,目前还有几个品种处于临床开发阶段(见表)。 (王宇恒)
